די יאָר'ס לאַסקער באַזיק מעדיצינישע פאָרשונג אַוואַרד איז געווען באַלוינט צו דעמיס האַסאַביס און דזשאַן דזשאַמפּער פֿאַר זייערע בייַשטייַער צו דער שאַפונג פון די אַלפאַפאָלד קינסטלעכע אינטעליגענץ סיסטעם וואָס פאָרויסזאָגט די דריי-דימענסיאָנאַלע סטרוקטור פון פּראָטעאינען באַזירט אויף דער ערשטער אָרדענונג סיקוואַנס פון אַמינאָ זויערן.
זייערע רעזולטאַטן לייזן אַ פּראָבלעם וואָס האָט לאַנג געפּלאָגט די וויסנשאַפטלעכע קהילה און עפֿענען די טיר צו באַשנעלערן פאָרשונג איבערן ביאָמעדיצינישן פעלד. פּראָטעאינען שפּילן אַ וויכטיקע ראָלע אין דער אַנטוויקלונג פֿון קראַנקייטן: אין אַלצהיימערס קראַנקייט, פֿאַלטן זיי זיך און קלאַמפּן זיך צוזאַמען; אין ראַק, גייט זייער רעגולאַטאָרישע פֿונקציע פֿאַרלוירן; אין געבוירענע מעטאַבאַלישע קרענק, זענען זיי דיספֿונקציאָנעל; אין סיסטיק פֿיבראָזיס, גייען זיי אין דעם אומרעכטן אָרט אין דער צעל. דאָס זענען נאָר אַ פּאָר פֿון די פֿילע מעכאַניזמען וואָס פֿאַראורזאַכן קראַנקייטן. דעטאַלירטע פּראָטעין סטרוקטור מאָדעלן קענען צושטעלן אַטאָמישע קאָנפיגוראַציעס, פֿירן דעם פּלאַן אָדער אויסוואַל פֿון הויך-אַפֿיניטי מאָלעקולן, און באַשנעלערן מעדיצין ענטדעקונג.
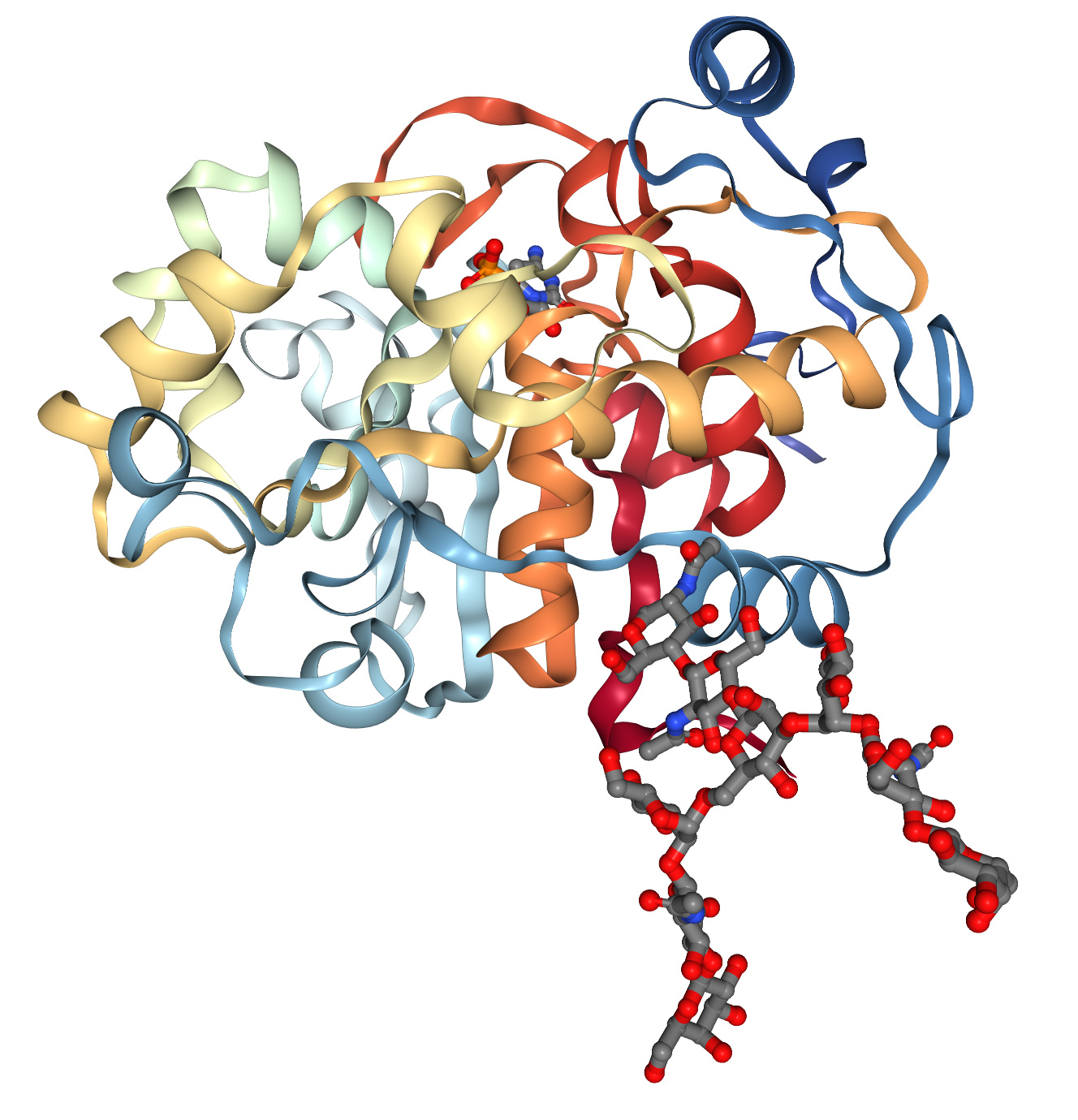
פּראָטעין סטרוקטורן ווערן בכלל באַשטימט דורך X-שטראַל קריסטאַלאָגראַפי, נוקלעאַר מאַגנעטיש רעזאָנאַנס און קריאָ-עלעקטראָן מיקראָסקאָפּי. די מעטאָדן זענען טייַער און צייט-פאַרנומענע. דאָס רעזולטאַט איז אַז עס עקזיסטירן 3D פּראָטעין סטרוקטור דאַטאַבייסעס מיט בלויז אַרום 200,000 סטרוקטורעלע דאַטן, בשעת DNA סיקוואַנסינג טעכנאָלאָגיע האט פּראָדוצירט מער ווי 8 מיליאָן פּראָטעין סיקוואַנסן. אין די 1960ער יאָרן, האָבן אַנפינסען און אַנדערע אַנטדעקט אַז די 1D סיקוואַנס פון אַמינאָ זויערן קען זיך ספּאָנטאַניש און ריפּיטיאַבלי פאָולדן אין אַ פאַנגקשאַנאַל דריי-דימענסיאָנאַל קאָנפאָרמאַציע (פיגור 1A), און אַז מאָלעקולאַרע "שאַפּעראָנען" קענען פאַרגיכערן און פאַסילאַטירן דעם פּראָצעס. די אָבסערוואַציעס פירן צו אַ 60-יאָר אַרויסרופן אין מאָלעקולאַרער ביאָלאָגיע: פאָרויסזאָגן די 3D סטרוקטור פון פּראָטעאינען פון די 1D סיקוואַנס פון אַמינאָ זויערן. מיטן הצלחה פון די מענטשלעכע גענאָם פּראָיעקט, איז אונדזער פיייקייט צו באַקומען 1D אַמינאָ זויער סיקוואַנסן שטאַרק פֿאַרבעסערט געוואָרן, און די אַרויסרופן איז געוואָרן נאָך מער דרינגלעך.
פאָרויסזאָגן פּראָטעין סטרוקטורן איז שווער פֿאַר עטלעכע סיבות. ערשטנס, אַלע מעגלעכע דריי-דימענסיאָנאַלע פּאָזיציעס פֿון יעדן אַטאָם אין יעדער אַמינאָ זויער פֿאָדערן אַ סך אויספֿאָרשונג. צווייטנס, פּראָטעאינען נוצן מאַקסימום קאָמפּלעמענטאַריטעט אין זייער כעמישער סטרוקטור צו עפֿעקטיוו קאָנפֿיגורירן אַטאָמען. זינט פּראָטעאינען האָבן טיפּיש הונדערטער וואַסערשטאָף בונד "דאָנאָרן" (געוויינטלעך זויערשטאָף) וואָס זאָלן זיין נאָענט צום וואַסערשטאָף בונד "אַקסעפּטאָר" (געוויינטלעך שטיקשטאָף געבונדן צו וואַסערשטאָף), קען עס זיין זייער שווער צו געפֿינען קאָנפֿאָרמאַציעס וווּ כּמעט יעדער דאָנאָר איז נאָענט צום אַקסעפּטאָר. דריטנס, עס זענען באַגרענעצטע ביישפּילן פֿאַר דער טריינינג פֿון עקספּערימענטאַלע מעטאָדן, אַזוי עס איז נייטיק צו פֿאַרשטיין די פּאָטענציעלע דריי-דימענסיאָנאַלע ינטעראַקשאַנז צווישן אַמינאָ זויערן אויף דער באַזע פֿון 1D סיקוואַנסן ניצן אינפֿאָרמאַציע וועגן דער עוואָלוציע פֿון די באַטייַטיקע פּראָטעאינען.
פיזיק איז ערשט גענוצט געוואָרן צו מאָדעלירן די אינטעראַקציע פֿון אַטאָמען אין דער זוכעניש פֿאַר דער בעסטער קאָנפאָרמאַציע, און אַ מעטאָדע איז דעוועלאָפּט געוואָרן צו פֿאָרויסזאָגן די סטרוקטור פֿון פּראָטעאינען. קאַרפּלוס, לעוויט און וואַרשעל זענען באַלוינט געוואָרן מיטן 2013 נאָבעל־פּריז אין כעמיע פֿאַר זייער אַרבעט אויף קאָמפּיוטיישאַנאַל סימולאַציע פֿון פּראָטעאינען. אָבער, פיזיק־באַזירטע מעטאָדן זענען קאָמפּיוטיישאַנאַל טייַער און דאַרפֿן אַפּראָקסימאַטיווע פּראַסעסינג, אַזוי פּינקטלעכע דריי־דימענסיאָנאַלע סטרוקטורן קענען נישט פֿאָרויסגעזאָגט ווערן. נאָך אַ "וויסן־באַזירטער" צוגאַנג איז צו נוצן דאַטאַבייסעס פֿון באַקאַנטע סטרוקטורן און סיקוואַנסן צו טרענירן מאָדעלן דורך קינסטלעכע אינטעליגענץ און מאַשין לערנען (AI-ML). האַסאַביס און דזשאַמפּער נוצן עלעמענטן פֿון ביידע פיזיק און AI-ML, אָבער די כידעש און שפּרונג אין פאָרשטעלונג פֿון דעם צוגאַנג שטאַמט בפֿרט פֿון AI-ML. די צוויי פֿאָרשער האָבן קרעאַטיוו קאָמבינירט גרויסע עפֿנטלעכע דאַטאַבייסעס מיט אינדוסטריעל־גראַד קאָמפּיוטינג רעסורסן צו שאַפֿן אַלפֿאַפאָלד.
ווי אזוי ווייסן מיר אז זיי האבן "געלייזט" די סטרוקטורעלע פאראויסזאגונג רעטעניש? אין 1994, איז געגרינדעט געווארן די קריטישע אפשאצונג פון סטרוקטור פאראויסזאגונג (CASP) קאנקורס, וואס טרעפט זיך יעדע צוויי יאר צו נאכפאלגן דעם פארשריט פון סטרוקטורעלע פאראויסזאגונג. די פארשער וועלן טיילן די 1D סיקווענץ פון דעם פראטעין וועמענס סטרוקטור זיי האבן לעצטנס אויפגעלייזט, אבער וועמענס רעזולטאטן זענען נאך נישט ארויסגעגעבן געווארן. דער פאראויסזאגער פאראויסזאגט די דריי-דימענסיאנעלע סטרוקטור ניצנדיג די 1D סיקווענץ, און דער אפשאצער באורטיילט אומאפהענגיק די קוואליטעט פון די פאראויסגעזאגטע רעזולטאטן דורך זיי צו פארגלייכן מיט די דריי-דימענסיאנעלע סטרוקטור צוגעשטעלט דורך דעם עקספערימענטאליסט (צוגעשטעלט נאר צום אפשאצער). CASP פירט דורך אמתע בלינדע באריכטן און רעקארדירט פעריאדישע פערפארמענס שפרינגען פארבונדן מיט מעטאדאלאגישע אינוואציע. ביי דער 14טער CASP קאנפערענץ אין 2020, האבן אלפאפאלד'ס פאראויסזאגונג רעזולטאטן געוויזן אזא שפרונג אין פערפארמענס אז די ארגאניזאטארן האבן געמאלדן אז די 3D סטרוקטור פאראויסזאגונג פראבלעם איז געלייזט געווארן: די גענויקייט פון רוב פאראויסזאגונגען איז געווען נאנט צו יענע פון עקספערימענטאלע מעסטונגען.
די ברייטערע באַדייטונג איז אַז האַסאַביס און דזשאַמפּער'ס אַרבעט ווייזט איבערצייגנדיק ווי AI-ML קען טראַנספאָרמירן וויסנשאַפֿט. איר פאָרשונג ווייזט אַז AI-ML קען בויען קאָמפּלעקסע וויסנשאַפֿטלעכע היפּאָטעזן פֿון קייפל דאַטן קוועלער, אַז אויפֿמערקזאַמקייט מעכאַניזמען (ענלעך צו די אין ChatGPT) קענען אַנטדעקן שליסל אָפּהענגיקייטן און קאָרעלאַציעס אין דאַטן קוועלער, און אַז AI-ML קען זיך אַליין משפט'ן די קוואַליטעט פֿון אירע רעזולטאַטן. AI-ML איז אין עסענץ טאָן וויסנשאַפֿט.
פּאָסט צייט: סעפּטעמבער 23, 2023